Los Mini Hígados Desarrollados por Científicos del MIT Ya Han Mostrado, en Estudios con Ratos, que Pueden Permanecer Activos Durante Ocho Semanas, Producir Sustancias Esenciales y Actuar como Apoyo Funcional a Un Hígado Comprometido, Abriendo Camino a Una Alternativa Menos Invasiva Ante la Escasez de Órganos Compatibles.
Los mini hígados desarrollados por ingenieros del MIT colocan en perspectiva una posibilidad que hasta poco tiempo parecía distante: crear injertos inyectables capaces de asumir parte de las funciones de un órgano comprometido sin exigir, de inmediato, un trasplante quirúrgico tradicional. En vez de sustituir completamente el hígado enfermo, la propuesta es ofrecer un refuerzo funcional al organismo.
Esta idea cobra fuerza porque el hígado desempeña un volumen impresionante de tareas esenciales para la supervivencia. Cuando este órgano pierde eficiencia, el impacto se expande por todo el cuerpo. Es justamente en este punto que los mini hígados pasan a llamar la atención, por haber demostrado, al menos en las pruebas iniciales, capacidad de producir enzimas y proteínas importantes durante semanas seguidas.
Lo que Hace que los Mini Hígados Sean Tan Relevantes en Este Momento
El avance llama la atención porque el hígado no es un órgano simple de apoyar artificialmente. Se trata del mayor órgano interno sólido del cuerpo humano y de una estructura responsable de cerca de 500 funciones fundamentales vinculadas a la regulación química de la sangre. Participa de procesos que van desde la coagulación hasta la eliminación de medicamentos y bacterias, lo que explica por qué la insuficiencia hepática suele ser tan grave.
-
Científicos finalmente descubrieron a dónde fue el plástico que desapareció de los océanos y la respuesta es aterradora: se fragmentó en partículas tan minúsculas que se volvieron invisibles y ahora son 27 millones de toneladas de nanoplástico solo en el Atlántico Norte.

-
La misión Artemis II llevará la cápsula Orion de vuelta al entorno de la Luna con cuatro astronautas, baño privado con cortina, sistema adaptado para hombres y mujeres y un nivel de confort que expone cuánto la era Apollo operaba en el límite más bruto de la exploración espacial.

-
Estructuras gigantes en el fondo del mar controlan el petróleo con precisión extrema y revelan cómo funcionan las válvulas submarinas de alta tecnología.

-
China acaba de probar un dron gigante del tamaño de un caza con 25 metros de envergadura que transporta 6 toneladas, vuela durante 12 horas y lo más aterrador: puede lanzar enjambres enteros de drones más pequeños directamente desde el aire.

Gran parte de este trabajo depende de los hepatocitos, células especializadas que ejecutan funciones centrales del hígado. A lo largo de la última década, el equipo liderado por investigadores del MIT ha estado buscando precisamente una forma de restaurar la actividad de estas células sin depender de una cirugía compleja. El objetivo no era solo crear tejido en laboratorio, sino hacer que este tejido sobreviva y opere dentro del cuerpo.
La importancia práctica de esto es evidente ante el número de pacientes que esperan un trasplante. El material informa que más de 10 mil americanos con enfermedad hepática crónica están en esta fila, en medio de la escasez de órganos compatibles. En este escenario, una solución intermedia, capaz de sostener al paciente hasta la llegada de un donante, ya representaría un cambio de enorme peso clínico.
Más que una promesa abstracta, los investigadores han comenzado a tratar estas estructuras como “hígados satélites”. La expresión ayuda a entender la lógica del proyecto: en vez de disputar espacio con el órgano enfermo o exigir su extracción, los injertos funcionarían como un apoyo adicional, reforzando lo que el cuerpo ya no puede hacer por sí solo.
Cómo Los Científicos Consiguieron Transformar Hepatocitos en Injertos Inyectables
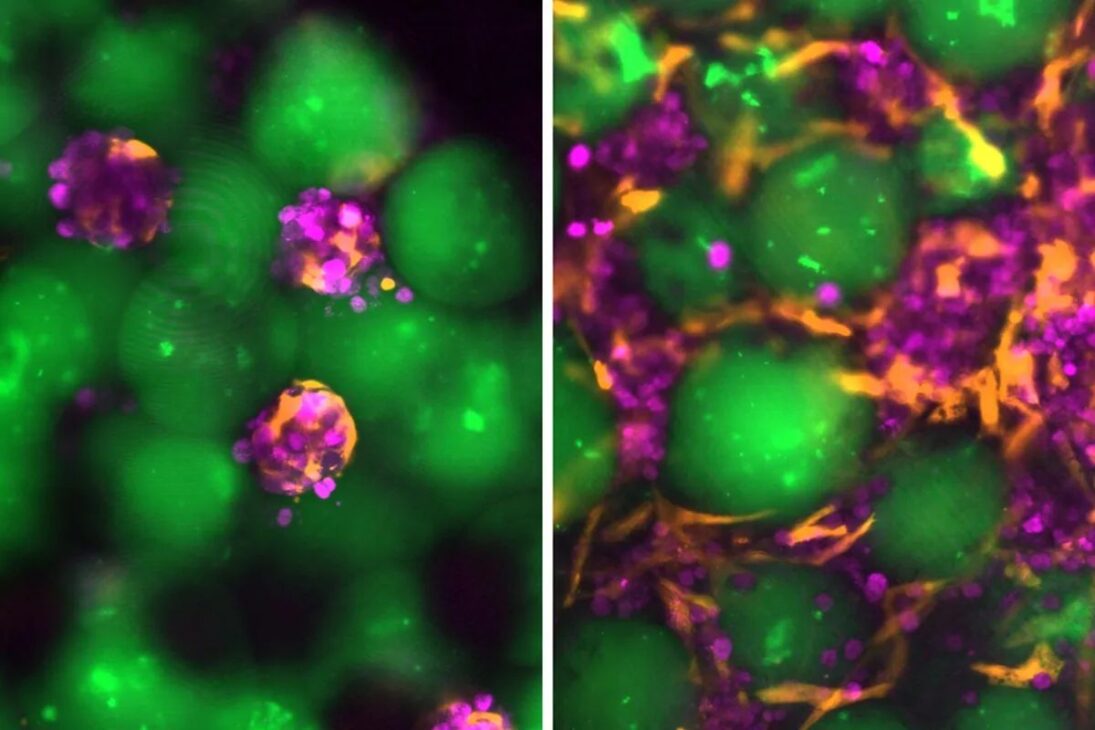
Una de las principales barreras estaba en la propia naturaleza del trasplante celular. En experiencias anteriores, una de las estrategias estudiadas fue incorporar hepatocitos a materiales biocompatibles, como hidrogeles. Estos materiales son redes tridimensionales de polímeros interconectados que pueden absorber gran volumen de agua sin disolverse, creando un ambiente favorable para las células.
El problema es que, aunque útiles para sostener los hepatocitos, los hidrogeles requerirían implantación quirúrgica. Esto colocaba la técnica de vuelta en el terreno de la cirugía invasiva, justamente lo que el equipo quería evitar. El gran cambio del proyecto fue encontrar una forma de inyectar no solo las células, sino todo el microambiente necesario para que sobrevivieran e integraran al organismo.
La solución involucró microesferas de hidrogel. Estas estructuras tienen un comportamiento particularmente interesante: cuando están compactadas, se comportan como un líquido y pueden aplicarse con jeringa; después de la inyección, recuperan la estructura sólida. Esta propiedad permitió unir dos necesidades que parecían difíciles de conciliar: aplicación mínimamente invasiva y sustentación física para las células trasplantadas.
En la práctica, estas microesferas ayudaron a los hepatocitos a permanecer agrupados, organizados y cerca de vasos sanguíneos. Esto es decisivo porque células aisladas, lanzadas en el cuerpo sin soporte, tienen muchas menos posibilidades de fijarse, recibir nutrientes y seguir funcionando. Sin nicho, la célula no se integra; con nicho, tiene una oportunidad real de permanecer viva y activa.
El Papel de las Microesferas y por Qué Hacen Tanta Diferencia
Las microesferas no funcionan solo como un vehículo de transporte. Crean un espacio favorable para que las células migren, se acomoden y formen un injerto estable. Este comportamiento ya se ha considerado prometedor incluso en cicatrización de heridas, porque facilita la ocupación de los espacios entre las esferas por nuevas células y tejido en formación.
En el caso de los mini hígados, este ambiente ayudó a los hepatocitos a hacer algo indispensable: conectarse rápidamente a la circulación del hospedador. Esto es central en cualquier intento de implante funcional, porque no basta con mantener la célula intacta. Necesita recibir nutrientes, intercambiar sustancias con el organismo y actuar de forma biológicamente útil.
Para aumentar aún más las posibilidades de éxito, los investigadores añadieron fibroblastos a la mezcla inyectable. Estas células de soporte contribuyeron a mejorar la supervivencia de los hepatocitos y estimular el crecimiento de vasos sanguíneos en el injerto. En otras palabras, el equipo no inyectó solo células hepáticas; montó un pequeño sistema de apoyo para que este tejido pudiera establecerse.
Este detalle ayuda a explicar por qué el estudio avanzó más allá de una simple prueba de concepto. Los nuevos vasos sanguíneos se formaron junto a los hepatocitos, permitiendo que reciban nutrientes directamente, continúen activos y produzcan las proteínas esperadas. Es esto lo que diferencia una célula presente en el cuerpo de una célula efectivamente funcional dentro del cuerpo.
Dónde Se Colocaron los Injertos y por Qué Esto Amplía el Potencial de la Técnica
En los experimentos realizados con ratones, los investigadores utilizaron el tejido adiposo en el abdomen como lugar de implantación. El procedimiento fue guiado por ultrasonido, tanto para posicionar la jeringa como para seguir la estabilidad del implante después de la aplicación. Esta elección muestra que la técnica no depende necesariamente del propio hígado como destino inmediato de las células.
Este es uno de los puntos más relevantes de la propuesta. Según el equipo, los injertos también podrían ser implantados en otras regiones del cuerpo, como el bazo y áreas cercanas a los riñones. Para la mayoría de las enfermedades hepáticas, el injerto no necesita permanecer junto al hígado para funcionar, siempre que encuentre espacio adecuado y tenga acceso a la circulación sanguínea.
Esta flexibilidad anatómica aumenta el interés clínico por la tecnología. En vez de quedar restringida a una única ventana quirúrgica o a un punto muy específico del organismo, la terapia puede ser pensada de forma más adaptable, considerando las condiciones del paciente y la viabilidad del procedimiento. Esto tiende a reducir obstáculos prácticos si el enfoque avanza a etapas futuras.
También hay un cambio importante de lógica terapéutica. En lugar de imaginar una reparación total e inmediata del órgano lesionado, la técnica propone una distribución funcional: células hepáticas actuando en otro punto del cuerpo, pero aun así ayudando en el metabolismo y en la producción de sustancias esenciales. Es una idea simple de entender y poderosa en sus implicaciones.
Lo que los Resultados en Ratos Revelaron Tras Ocho Semanas
El dato más fuerte presentado hasta aquí es el tiempo de actividad observado en el estudio. Las células de hepatocitos inyectadas permanecieron operativas durante todo el período analizado, que llegó a ocho semanas. Durante ese intervalo, los injertos produjeron con éxito muchas de las enzimas y proteínas normalmente fabricadas por hígados reales.
Esto importa porque una prueba demasiado corta podría indicar solo supervivencia transitoria. Aquí, sin embargo, el comportamiento registrado sugiere continuidad funcional a lo largo de un período relevante para un estudio inicial. El injerto no solo permaneció en el organismo, sino que continuó trabajando. Esta distinción es crucial para evaluar el potencial de la tecnología como tratamiento a largo plazo.
Aún se trata de un resultado en animales, y esto debe mantenerse en perspectiva. El rendimiento en ratones no garantiza la misma respuesta en humanos, ni permite concluir que la aplicación clínica está cerca. Pero los hallazgos dan sustento concreto a la hipótesis de que los injertos inyectables pueden servir como apoyo duradero a la función hepática.
También llama la atención el hecho de que la propuesta no esté restringida a casos de sustitución definitiva. Los propios investigadores ven la tecnología como un posible puente hacia el trasplante. Esto significa ofrecer soporte funcional temporal hasta que un órgano donante compatible esté disponible, lo que puede ser decisivo en situaciones de espera prolongada.
Quién Puede Beneficiarse Más si la Técnica Avanza a Uso Clínico
El grupo más directamente beneficiado sería el de los pacientes con enfermedad hepática crónica que dependen de trasplante y enfrentan escasez de órganos. Para estas personas, cualquier terapia capaz de estabilizar funciones del cuerpo por más tiempo puede representar la diferencia entre resistir hasta la llegada de un donante o agravarse antes de eso.
Pero hay otro grupo que puede ganar espacio en esta discusión: los pacientes que no son considerados elegibles para trasplante porque están demasiado frágiles para tolerar una cirugía. En esos casos, un enfoque inyectable y menos invasivo podría abrir una alternativa donde hoy existen limitaciones severas. Este punto amplía mucho el alcance potencial de la tecnología, porque no se trata solo de reducir la lista de espera, sino también de incluir perfiles antes excluidos.
Los investigadores destacan aún otra ventaja: si se necesitan nuevos injertos o terapias complementarias, la barrera para repetir el procedimiento tiende a ser menor que la de una nueva cirugía. Esto modifica la estrategia de cuidado al transformar el tratamiento en algo posiblemente más ajustable a lo largo del tiempo.
En vez de una única intervención radical, lo que se perfila es un enfoque escalonado. El paciente podría recibir soporte, ser reevaluado y, conforme a la respuesta clínica, pasar por nuevas aplicaciones con menos impacto que una intervención quirúrgica convencional. Este razonamiento hace de los mini hígados no solo un experimento curioso, sino una propuesta terapéutica con lógica práctica.
Los Límites Actuales y lo que Aún Necesita Ser Resuelto
A pesar del avance, la tecnología aún enfrenta obstáculos relevantes. En el concepto actual, los pacientes necesitarían usar medicamentos inmunosupresores para recibir los mini hígados. Este punto es importante porque el rechazo inmunológico continúa siendo un desafío central en terapias celulares y trasplantes.
En el futuro, el equipo evalúa dos posibilidades para sortear este problema. Una de ellas sería desarrollar hepatocitos «furtivos», capaces de escapar del rechazo inmunológico. La otra sería adaptar las microesferas de hidrogel para liberar inmunosupresores directamente en el lugar de la inyección, concentrando el efecto donde es necesario.
Las dos estrategias muestran que los investigadores no están mirando solo para el éxito inicial del implante, sino también para la viabilidad clínica del tratamiento en escenarios reales. Aún así, hay una distancia importante entre el buen rendimiento en laboratorio y la adopción a gran escala en pacientes humanos. Esta distancia involucra seguridad, eficacia, durabilidad y control de la respuesta inmune.
Por eso, el avance debe ser visto con entusiasmo moderado. Hay razones objetivas para atención y expectativa, pero también hay etapas indispensables antes de que esta tecnología deje de ser un resultado experimental y pase a integrar la atención médica cotidiana.
Por Qué los Mini Hígados Despiertan Tanta Expectativa en la Medicina
Los mini hígados atraen interés porque reúnen, en un único proyecto, tres elementos que raramente aparecen juntos con tanto equilibrio: aplicación menos invasiva, función biológica real y potencial de uso como soporte prolongado. No se trata solo de mantener células vivas en laboratorio, sino de hacer que actúen como tejido funcional dentro del organismo.
Esta combinación ayuda a explicar por qué el tema parece ficción a primera vista. La idea de inyectar pequeños injertos capaces de producir proteínas y enzimas como un órgano real suena extraordinaria. Pero lo que hace la historia relevante no es el impacto visual de la propuesta, sino su coherencia biológica y clínica. Los mini hígados fueron pensados para resolver un problema concreto: cómo sostener pacientes cuando el trasplante no puede ocurrir inmediatamente.
Si los próximos pasos confirman este potencial, la tecnología podría ocupar un espacio valioso entre el tratamiento convencional y el trasplante completo. Este espacio, hoy, es justamente donde muchos pacientes siguen vulnerables, esperando por tiempo, compatibilidad y condiciones clínicas favorables.
A partir de ahí, la medicina hepática puede ganar una nueva herramienta: no la sustitución inmediata del órgano, sino un refuerzo funcional diseñado para salvar tiempo, preservar estabilidad y ampliar posibilidades terapéuticas. Y eso, por sí solo, ya es un horizonte transformador.
La creación de los mini hígados por el MIT muestra cómo la ingeniería biomédica ha estado intentando responder a uno de los problemas más difíciles de la medicina hepática: ofrecer soporte real a un organismo debilitado sin depender exclusivamente de una cirugía de gran porte.
Los resultados iniciales en ratones aún no cierran esta historia, pero ya cambian la forma de ver lo que puede ser posible en los próximos años.
Cuando una tecnología logra unir precisión biológica, aplicación inyectable y actividad funcional durante semanas, deja de ser solo una curiosidad científica y merece atención seria. Entre la urgencia de los pacientes y la escasez de órganos, los mini hígados surgen como una posibilidad que, por primera vez, parece concreta.
¿Crees que terapias inyectables así pueden cambiar el futuro de los trasplantes o sigue existiendo un largo camino hasta que esto se haga realidad?

 Portugués
Portugués  Inglés
Inglés  Español
Español 











Eu acredito sim, a medicina está muito avançada meus parabéns.