Investigadores de la Universidad del Sur de California han creado células madre de nefronas de larga duración que crecen de forma estable en laboratorio y se organizan en organoides renales tridimensionales capaces de filtrar como un riñón real, abriendo camino para estudiar enfermedades genéticas, probar medicamentos y, en el futuro, construir riñones artificiales para los más de 94 mil estadounidenses en la lista de espera de trasplante
Investigadores de la Universidad del Sur de California (USC) anunciaron un avance que puede cambiar el futuro del tratamiento de enfermedades renales. Han logrado crear células madre de nefronas que crecen de forma estable y por un tiempo prolongado en laboratorio, algo que hasta ahora era uno de los mayores obstáculos de la medicina regenerativa renal. Estas células son el material inicial que construye las nefronas, las unidades de filtración de los riñones, y los investigadores las utilizaron para formar organoides: mini estructuras tridimensionales que imitan el funcionamiento de un riñón real.
El descubrimiento no significa que riñones de laboratorio listos para trasplante estén en camino mañana. Pero significa que los investigadores ahora tienen una herramienta más robusta y escalable para cultivar células renales, estudiar enfermedades genéticas como la enfermedad renal poliquística y probar medicamentos con una precisión mucho mayor que antes. Para los más de 94 mil estadounidenses que estaban en la lista de espera para trasplante de riñón en diciembre de 2025, y para los millones de pacientes en diálisis en el mundo, cualquier avance en esta dirección es concreto. El estudio fue publicado en la revista Cell Stem Cell.
Lo que los investigadores de la USC lograron hacer con células renales

Cada riñón humano contiene alrededor de un millón de nefronas, estructuras microscópicas que filtran la sangre, eliminan residuos y equilibran agua y minerales. Cuando las nefronas fallan en número suficiente, el riñón deja de funcionar y el paciente necesita diálisis o trasplante.
-
Iban a construir una carretera, pero acabaron encontrando en la República Checa una ciudad celta entera soterrada desde hace más de 2 mil años, con cientos de monedas de oro y plata, ámbar precioso y uno de los mayores tesoros arqueológicos jamás descubiertos.

-
Arqueólogos encuentran ciudad medieval perdida en Polonia con plaza central, cementerio, forja y más de 500 artefactos enterrados.

-
Una masa de aire caliente gigantesca se extendió desde Brasil hasta cerca de la Antártida y provocó algo que casi nunca sucede: rayos y truenos en Ushuaia, en las Islas Malvinas y en las Islas Georgia del Sur.

-
Mayor que un campo de fútbol, con 117 metros de envergadura, seis motores de Boeing 747 y capacidad para 250 toneladas, el Stratolaunch Roc transforma el cielo en una gigantesca rampa de lanzamiento hipersónico y acelera la forma en que EE. UU. prueba armas de Mach 5 a Mach 10.

Lo que los investigadores de la USC hicieron fue cultivar las células que construyen estas nefronas de tal manera que continuaran creciendo y multiplicándose en laboratorio por un tiempo prolongado, sin perder la capacidad de organizarse en estructuras funcionales.
Para lograr esto, los investigadores ajustaron la señalización de dos proteínas llamadas p38 y YAP, que funcionan como interruptores internos de las células. Al manipular estos interruptores, mantuvieron las células en un estado flexible y progenitor, capaz de continuar dividiéndose.
El resultado fue la expansión a largo plazo de células madre de nefronas tanto de ratones como de humanos, incluyendo versiones derivadas de células madre pluripotentes humanas que pueden ser creadas a partir de una simple biopsia de sangre o piel.
Los organoides renales que los investigadores crearon y por qué son diferentes
Los organoides renales ya existían antes de este estudio, pero la mayoría de los protocolos generaban un problema: junto con las células renales deseadas, aparecían células no deseadas como neuronas y fibras musculares.
Los organoides creados por los investigadores de la USC presentaron solo un 0,67% de células fuera del objetivo en análisis de célula única, un número drásticamente menor que los protocolos anteriores. Esto significa mini estructuras más puras y más parecidas con un riñón de verdad.
Los organoides también mostraron una maduración más acentuada de los podocitos, células especializadas que ayudan a filtrar la sangre dentro de la nefrona. Y los investigadores descubrieron algo inesperado: el medio de cultivo logró inducir a podocitos maduros a revertir a un estado similar al de células madre.
Esta plasticidad de las células renales era algo que los investigadores no habían comprendido antes, y puede abrir nuevas posibilidades para regenerar tejido renal dañado.
Cómo los investigadores ya están usando las células para probar medicamentos
Como las células crecieron más y se volvieron más fáciles de editar genéticamente, los investigadores pudieron usarlas para cribado genómico por CRISPR. Esta técnica permitió identificar genes relacionados con el desarrollo y las enfermedades renales, incluyendo genes ya sospechosos y nuevos candidatos que no habían sido asociados al riñón antes.
Es exactamente el tipo de plataforma que los investigadores necesitan cuando quieren entender cómo comienza una enfermedad renal y qué objetivos moleculares pueden ser atacados con medicamentos.
Los investigadores también modelaron la enfermedad renal poliquística autosómica dominante (DRPAD), la enfermedad renal hereditaria más común, y evaluaron 148 compuestos en cuanto a los efectos en la formación de quistes.
Catorce mostraron una inhibición significativa, 12 mantuvieron eficacia en una segunda ronda y el PTC-209 se destacó como un inhibidor que no había sido previamente asociado a la supresión de quistes de la DRPAD.
Para los investigadores, esta capacidad de probar cientos de compuestos en organoides renales puros y editables es lo que transforma el descubrimiento en una herramienta práctica para la industria farmacéutica.
Lo que aún falta para que los investigadores construyan un riñón artificial completo
Los investigadores son claros sobre las limitaciones. Los organoides son mini estructuras cultivadas en laboratorio, no riñones artificiales completos listos para trasplante.
Aún falta generar toda la gama de tipos de células de la nefrona, especialmente estructuras como las asas de Henle y los túbulos contorneados distales, componentes esenciales para que un riñón artificial funcione como el órgano real.
Pero el avance es significativo porque resuelve un problema que había paralizado la investigación durante años: la dificultad de obtener células renales confiables en cantidad suficiente para estudio y edición genética.
Zhongwei Li, autor principal del estudio, afirmó que al mejorar la capacidad de cultivar estas células, los investigadores han creado una nueva vía para comprender y combatir enfermedades renales congénitas y cáncer.
La enfermedad renal crónica afecta a más de 1 de cada 7 adultos en los Estados Unidos, y para estos pacientes, cada paso hacia un riñón artificial o hacia medicamentos más eficaces es un paso lejos de la diálisis.
Células que se niegan a morir y un futuro sin diálisis
Investigadores de la USC han creado células renales que crecen de forma estable en laboratorio, se organizan en mini estructuras que imitan el riñón real y ya están siendo utilizadas para probar medicamentos contra enfermedades renales hereditarias.
No es un riñón artificial listo para trasplante, pero es la base sobre la cual este riñón puede ser construido en el futuro, y para los millones de pacientes que dependen de la diálisis, el mensaje de los investigadores es que la ciencia está avanzando en la dirección correcta.
¿Conoces a alguien que dependa de diálisis? ¿Crees que veremos riñones artificiales funcionando en humanos aún en esta década? ¿Qué piensas sobre el avance de los investigadores de la USC? Déjanos tus comentarios y comparte este artículo con quienes siguen la ciencia y la salud.

 Portugués
Portugués  Inglés
Inglés  Español
Español 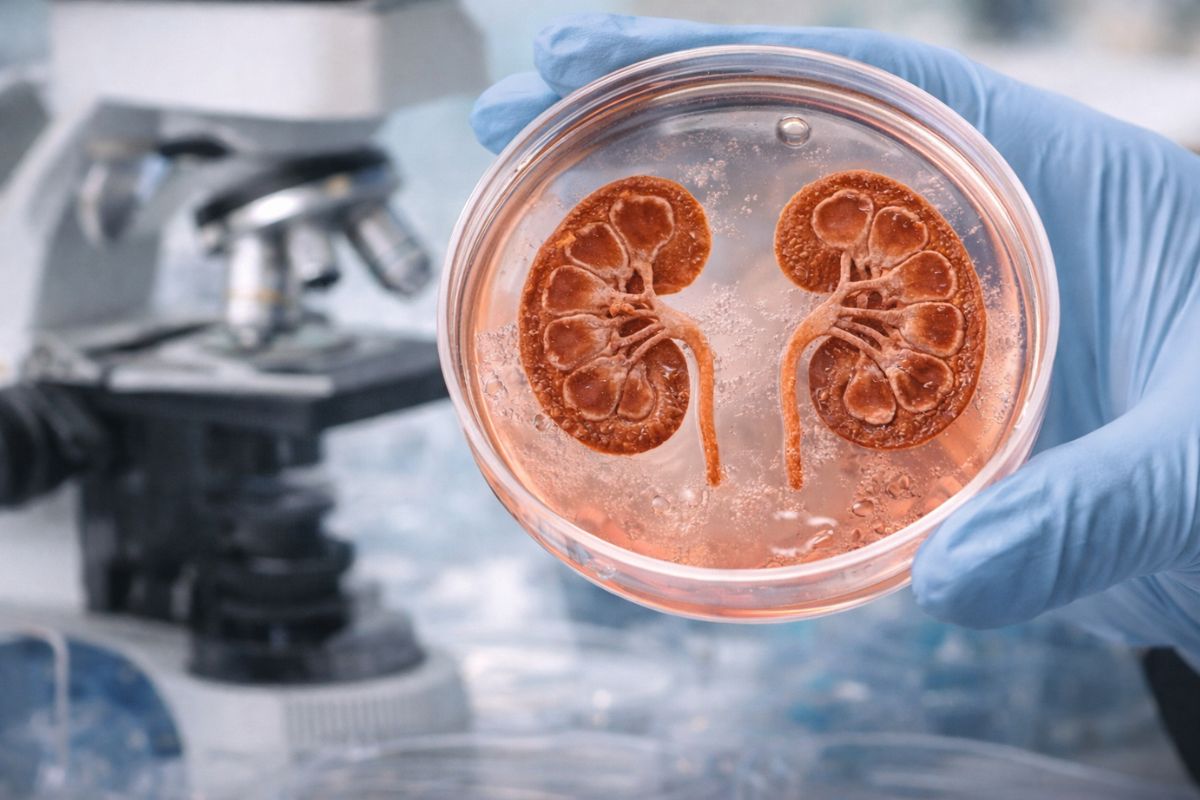





Seja o primeiro a reagir!