Estudio publicado en Nature Cell Biology muestra cómo la vitamina B2 ayuda a células cancerígenas a escapar de la ferroptosis y señala a la roseoflavina como objetivo terapéutico.
Según ScienceDaily, investigadores del Rudolf Virchow Centre, de la Julius-Maximilians-Universität Würzburg, en Alemania, publicaron el 13 de marzo de 2026, en Nature Cell Biology, un descubrimiento que cambia la forma en que la ciencia observa la relación entre la vitamina B2, las células cancerígenas y la ferroptosis. El estudio reveló que la riboflavina, nombre técnico de la vitamina B2, desempeña un papel crucial en la protección de células tumorales contra una forma específica de muerte celular programada.
La investigación fue liderada por Vera Skafar, estudiante de doctorado del grupo del profesor José Pedro Friedmann Angeli. Según ella, la vitamina B2 ayuda a células cancerígenas a resistir la ferroptosis, un mecanismo natural usado por el organismo para eliminar células con daños oxidativos graves.
El punto central del estudio es la proteína FSP1, Ferroptosis Suppressor Protein 1, identificada como enlace decisivo de este sistema de defensa. En las células saludables, el mecanismo es útil; en las células cancerígenas, sin embargo, puede ser explotado por el tumor para escapar de la destrucción natural.
-
Dentro de la olla a presión, el experimento muestra cómo el vapor aumenta la temperatura, acelera la cocción del frijol y además explica por qué una válvula obstruida puede transformar un utensilio común en un riesgo doméstico.
-
Sin aire acondicionado, sin gas refrigerante y usando solo tubos enterrados en el patio, un hombre construye un sistema geotérmico inspirado en el «pozo canadiense» para enfriar las habitaciones de la casa aprovechando la temperatura estable del subsuelo y elimina ventiladores en las noches más calurosas.
-
Brasil quiere convertirse en potencia militar con más de 2.100 blindados para 2040, cañones de 120 mm capaces de alcanzar objetivos a 5 km, vehículos anfibios a 110 km/h y una nueva flota multimillonaria del Ejército Brasileño lista para modernizar el combate terrestre.
-
Plástico que iría para vertederos se convierte en gasolina, diésel y queroseno en México, pero la tecnología de Petgas abre disputa: ¿reciclaje real o una forma más limpia de quemar basura mientras la contaminación plástica crece en el mundo a una escala global urgente?
La vitamina B2 ayuda a células cancerígenas a escapar de la ferroptosis, revela estudio publicado en Nature Cell Biology
El descubrimiento no significa que la vitamina B2 cause cáncer, pero muestra que células tumorales pueden usar la riboflavina como soporte metabólico para sobrevivir. La vitamina participa en procesos normales del cuerpo, pero, en tumores, puede alimentar una ruta de protección contra la ferroptosis.
La ferroptosis es una forma de muerte celular programada basada en daño oxidativo en las membranas celulares. Cuando este daño supera las defensas antioxidantes de la célula, la membrana se degrada progresivamente y la célula muere.
El estudio mostró que células cancerígenas pueden reforzar este escudo de protección con ayuda de la vitamina B2. Este detalle es relevante porque muchos tumores agresivos dependen precisamente de sistemas antioxidantes fuertes para resistir la muerte celular.
¿Qué es la ferroptosis y por qué este mecanismo puede ayudar al cuerpo a destruir tumores?
La muerte celular programada es un proceso utilizado por el organismo para eliminar células dañadas, infectadas o potencialmente peligrosas. La forma más conocida es la apoptosis, objetivo de muchos tratamientos convencionales contra el cáncer.
La ferroptosis sigue otro camino. Ocurre cuando reacciones que involucran hierro y lípidos provocan peroxidación lipídica, dañando las membranas celulares hasta que la célula ya no pueda sobrevivir.
Este mecanismo ha despertado interés porque puede alcanzar tumores que han desarrollado resistencia a la apoptosis. En lugar de depender solo de la respuesta tradicional a quimioterápicos, la ferroptosis abre una ruta alternativa para matar células cancerígenas resistentes.
La proteína FSP1 funciona como escudo contra ferroptosis y puede ser explotada por el cáncer
La proteína FSP1 fue identificada como pieza central del mecanismo descrito por los investigadores de Würzburg. Existe en las células saludables para evitar la muerte celular accidental causada por daño oxidativo.
En las células normales, esta función es importante. Impide que tejidos saludables sufran ferroptosis sin necesidad, protegiendo al organismo contra daños indebidos.
El problema es que las células cancerígenas pueden explotar la misma proteína para sobrevivir. Al usar la FSP1 como escudo, el tumor reduce su vulnerabilidad a uno de los mecanismos naturales de eliminación celular.
La riboflavina sustenta la actividad de la FSP1 y fortalece la defensa de las células tumorales
La vitamina B2 entra en este proceso porque es convertida por el metabolismo en cofactores que ayudan a sustentar la actividad de la FSP1. De esta forma, la riboflavina participa indirectamente en la protección contra ferroptosis.
Cuando los investigadores crearon células cancerígenas deficientes en vitamina B2 mediante edición genómica, estas células se volvieron mucho más sensibles a la ferroptosis. Sin suficiente riboflavina, el sistema de defensa perdió fuerza.
El resultado fue directo: al reducir el soporte metabólico de la vitamina B2, los científicos lograron hacer que las células tumorales fueran más vulnerables a la muerte celular programada. Este es el punto que transforma el descubrimiento en un posible camino terapéutico.
Roseoflavina, compuesto bacteriano, puede desactivar el escudo protector de las células cancerígenas
La parte más prometedora del estudio aparece en la roseoflavina, un compuesto producido naturalmente por bacterias, especialmente la Streptomyces davawensis. La molécula es estructuralmente parecida con la riboflavina, lo que permite su entrada en la célula por vías similares.
Una vez dentro de la célula, la roseoflavina se une a la proteína FSP1 e interfiere en su función protectora. El compuesto impide que la proteína cumpla su papel normal de bloquear la ferroptosis en las células cancerígenas.
En las pruebas con modelos celulares, este bloqueo redujo la protección tumoral. Sin FSP1 funcional, las células cancerígenas quedaron más expuestas a la ferroptosis, abriendo camino para una estrategia terapéutica basada en desactivar la defensa del tumor.
El descubrimiento no significa que la vitamina B2 cause cáncer o deba ser evitada en la dieta
La interpretación correcta del estudio es esencial. La investigación no demostró que consumir vitamina B2 cause cáncer, aumente el riesgo de tumor o deba ser evitada por personas saludables.
La riboflavina es una vitamina esencial que el cuerpo humano no produce en cantidad suficiente por sí solo. Necesita venir de la alimentación, a través de fuentes como leche, huevos, carnes, espinacas, champiñones y granos enriquecidos.
El hallazgo se refiere a células que ya se han vuelto cancerígenas. La vitamina B2 no se presenta como causa del cáncer, sino como un recurso metabólico que algunos tumores pueden usar para protegerse de la ferroptosis.
Bloquear el metabolismo de la vitamina B2 en el tumor es diferente de retirar riboflavina de la alimentación
La implicación terapéutica del estudio no es reducir la vitamina B2 de la dieta. Esta medida podría perjudicar células saludables, ya que la riboflavina participa en funciones metabólicas importantes en el organismo.
El objetivo real es bloquear selectivamente la vía de la vitamina B2 dentro de las células tumorales. La roseoflavina aparece como candidata justamente porque logra interferir en el sistema que sostiene la FSP1.
La estrategia ideal sería atacar el tumor sin afectar el metabolismo normal de las células saludables. Este desafío de especificidad es una de las principales etapas que los investigadores aún necesitan superar antes de cualquier aplicación clínica.
La ferroptosis se ha convertido en un objetivo prometedor contra tumores resistentes a tratamientos convencionales
El campo de la ferroptosis es relativamente nuevo en la biomedicina. El mecanismo fue descrito en detalle solo en 2012, y los primeros estudios sobre su inducción específica en tumores ganaron fuerza entre 2014 y 2016.
El interés creció porque muchos cánceres aprenden a resistir a los tratamientos basados en apoptosis. Cuando esto sucede, los tumores pueden escapar de terapias tradicionales y continuar creciendo incluso bajo presión medicamentosa.
La ferroptosis ofrece una ruta diferente. Al explorar vulnerabilidades oxidativas de las células cancerígenas, los investigadores buscan nuevas formas de atacar tumores que ya no responden bien a mecanismos clásicos de muerte celular.
Estudio de la Universidad de Würzburg conecta la vitamina B2 a la resistencia tumoral por primera vez
El estudio de Würzburg es importante porque conecta directamente el metabolismo de la vitamina B2 a la resistencia de células cancerígenas contra la ferroptosis. Esta conexión aún no había sido descrita con este nivel de claridad.
La investigación fue financiada por el programa prioritario Ferroptosis: from Molecular Basics to Clinical Applications, de la Fundación Alemana de Investigación, y por el proyecto DeciFerr, coordinado por el profesor Friedmann Angeli y apoyado por el Consejo Europeo de Investigación.
Esta financiación muestra que la ferroptosis ya se trata como un campo estratégico para aplicaciones clínicas futuras. El descubrimiento de la relación entre riboflavina, FSP1 y roseoflavina añade una nueva ruta posible para terapias anticáncer.
El próximo desafío es llevar la roseoflavina al tumor sin afectar células saludables
A pesar del potencial, la investigación aún está en etapa experimental. Los resultados provinieron de modelos celulares, y aún será necesario probar seguridad, eficacia, entrega selectiva y efectos en organismos vivos.
El desafío central es desarrollar formas de llevar la roseoflavina, o compuestos similares, específicamente a las células tumorales. Como la vitamina B2 también es esencial para células saludables, cualquier intervención necesita evitar efectos secundarios amplios.
El descubrimiento es fuerte porque revela un mecanismo nuevo y una vulnerabilidad posible. Pero aún no se trata de un tratamiento disponible para pacientes, sino de una ruta científica prometedora que necesita pasar por nuevas fases de validación.
Vitamina B2, FSP1 y roseoflavina abren una nueva frente en la investigación contra el cáncer
El estudio publicado en Nature Cell Biology muestra cómo un nutriente esencial puede tener un papel doble en el organismo. En las células saludables, la riboflavina sostiene funciones necesarias; en las células cancerígenas, puede fortalecer una defensa contra la ferroptosis.

La identificación de la FSP1 como un enlace central y de la roseoflavina como un posible bloqueador del escudo tumoral crea una nueva hipótesis terapéutica. En lugar de atacar indiscriminadamente las células, la estrategia busca desactivar la protección que impide que el tumor muera por un proceso natural.
El avance no autoriza conclusiones apresuradas sobre la dieta ni sustituye tratamientos existentes. Pero revela una dirección importante: entender cómo el cáncer utiliza mecanismos normales del cuerpo contra el propio organismo puede ser el camino hacia terapias más precisas y menos agresivas en el futuro.

 Español
Español 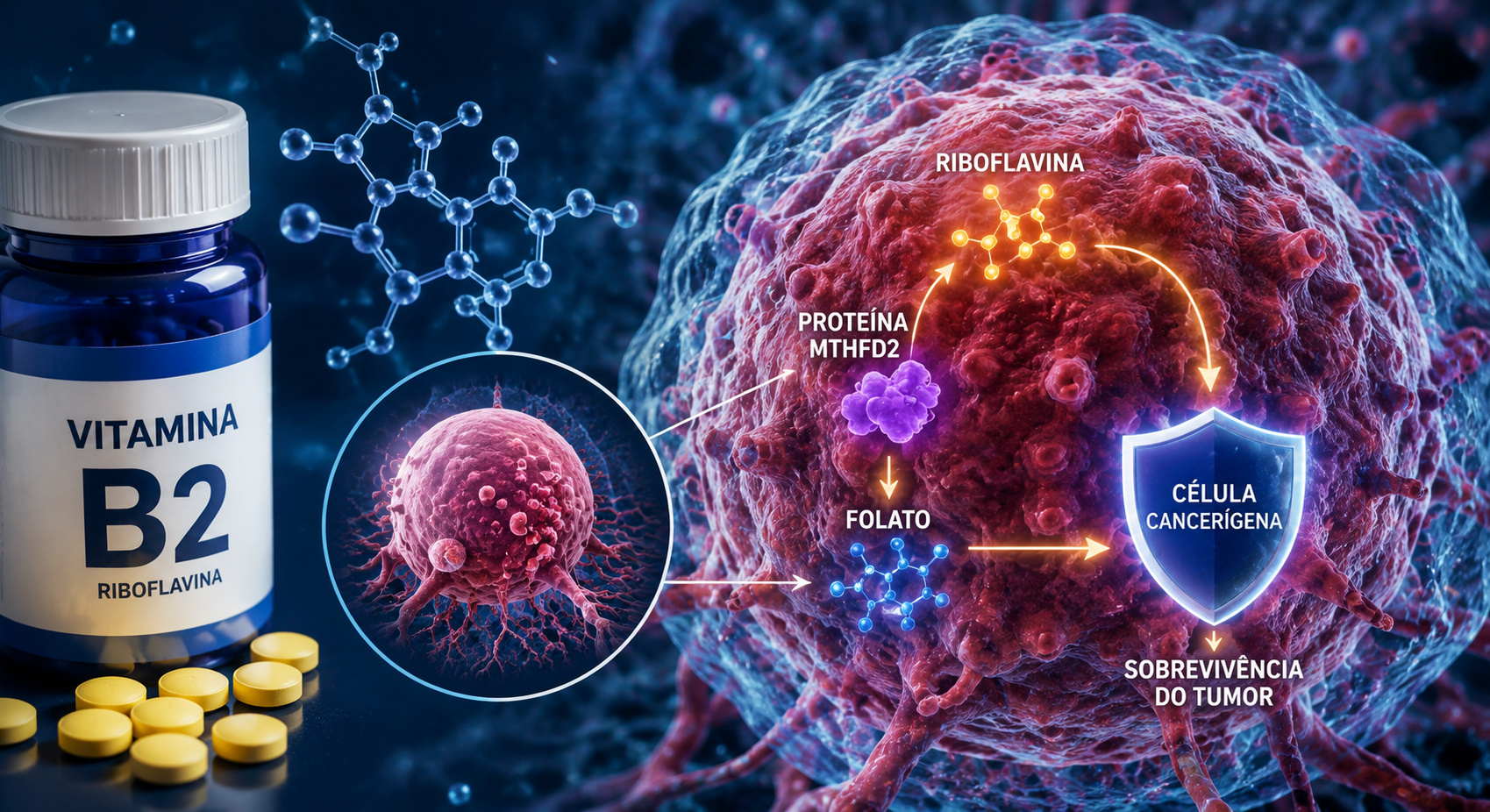













 Comment Author Info
Comment Author Info
¡Sé la primera persona en reaccionar!